“耀杰不凡”致敬幕后抗疫英雄推文解讀活動
第一刊:ddPCR比拼RT-PCR,探最精準新冠載量變化
疫情之下,逆行者最美,守護人民健康,貢獻智慧與光芒,國內首批獲證新型冠狀病毒核酸檢測試劑盒知名生產廠家伯杰醫療特發起《“耀杰不凡”——致敬幕后抗疫英雄系列》學術專題活動。旨在傳播、分享疫情期間一線檢驗及臨床工作者相關研究成果,經過論文征集及篩查,最終確定病毒載量、婦兒感染、混合感染、病毒結構、樣本差異、輸入防控、出院復陽、試劑盒優劣等8期內容進行分享。


本期研究由首都醫科大學附屬北京地壇醫院張福杰教授團隊基于清華大學郭永研究員團隊的微液滴數字PCR(ddPCR)研究完成,通過對比ddPCR和RT-PCR技術在新冠患者疾病進展中病毒載量的變化,發現并證明了使用RT-PCR和ddPCR定量檢測下的病毒載量對于評估疾病的進展有積極作用,而在病毒載量低的情況下,其優勢更是顯著。
本期作者團隊之一來自北京地壇醫院,他們在整個疫情期間,救治了大量的新冠患者,在北京防疫期間承擔著非常重要的工作,而這項研究成果也誕生在這個時期。

研究共納入了127例患者的400個樣本,首都醫科大學附屬北京地壇醫院張福杰教授團隊與清華大學郭永研究員團隊在設計實驗之初,為了達到更好的對比評估效果,不僅使用RT-PCR和ddPCR同時去檢測標本,實驗所招募的127名受試者也既包括確診病例54例、疑似病例39例,同時又納入了34例因發燒或呼吸道癥狀接收篩查但不符合可疑病例診斷標準的患者。患者包括:具有1次接觸史及2種臨床情況;無明確的接觸史,但符合3種臨床情況。(臨床情況包含:發燒和/或呼吸道癥狀,病毒性肺炎的影像學特征,發病初期較早的白細胞計數正常或低,淋巴細胞計數減少)
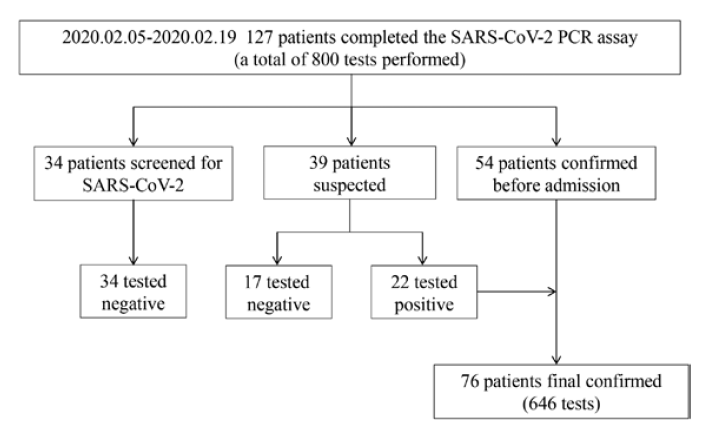
圖1. 項目檢測參與者構成圖
SARS-CoV-2檢測:
本次研究所涉及的樣本類型較為全面,包括了口咽拭子,鼻咽拭子,痰液,血液和尿液樣本,統一采用專業的核酸提取試劑盒在2個小時內完成核酸提取,然后再進行RT-PCR和ddPCR檢測。
其中RT-PCR檢測使用上海伯杰醫療科技有限公司的反應和擴增系統,對靶向ORF1ab和N基因以及陽性參考的引物和探針進行了逆轉錄PCR。
檢測結果:
數據分析:通過RT-PCR和ddPCR兩種方法的檢測,34例篩查病例和17例可疑病例的77份標本結果均呈陰性。從患者年齡上看,中位年齡為40歲,男性比例為50%;入院時最常見的體征和癥狀是發燒和咳嗽。
從病程進展看,77.6%的患者為輕度類型,而22.4%的患者為較嚴重類型。從臨床階段而言,有49例患者處于恢復階段,所占比例最大,其次是進行性階段,早期階段和臨床治愈階段。7名患者的胸部影像學正常,因此處于不確定的階段。從癥狀發作到發病初期,進展階段和恢復階段的平均天數分別為疾病發作后的4天,12天和20天。
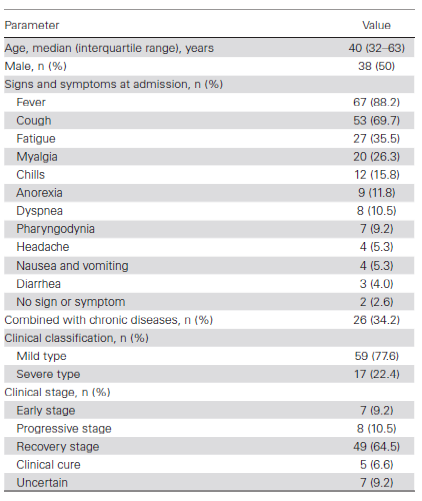
圖2. 最終確診患者的癥狀
兩種檢測方法對另外76名確診患者的323個樣本檢測結果則顯示:根據RT-PCR結果,95例陽性,67例單基因陽性,161例陰性。95例陽性的ddPCR結果也均為陽性,RT-PCR的Ct值與病毒載量高度相關。在67個單基因陽性樣品中,ddPCR陰性的有26個,陽性的有41個陽性,拷貝數范圍為11.1至123.2拷貝/測試。
剩余161個RT-PCR陰性樣本中,有157個樣本的ddPCR檢測結果為陰性,4個樣本陽性。結果表明,RT-PCR和ddPCR在高病毒載量樣品和陰性樣品中均準確可靠。然后,我們進一步比較了3個呼吸道樣本中的病毒載量。痰液中的平均病毒載量(17429±6920拷貝/測試)顯著高于口咽拭子和鼻咽拭子。
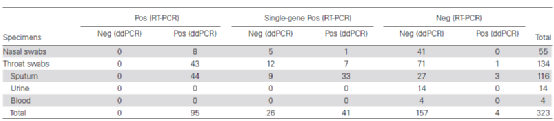
圖3. RT-PCR和ddPCR的樣本結果

此次研究表明,RT-PCR和ddPCR對高病毒載量樣品給出了一致的結果。不同樣本類型的病毒載量顯示,痰液樣本中的病毒比口咽拭子和鼻咽拭子要多。痰液樣本的定量結果與最近報道的研究一致:病毒載量在早期和進行性階段呈現增加趨勢,而在恢復階段則出現下降。恢復的患者可能會出現間歇性病毒脫落,導致核酸結果再次呈陽性。隨著時間的流逝,大量患者將進入康復階段并出院,對低病毒載量的監測將更加頻繁。下呼吸道樣品的多次測試以及通過不同方法進行的測試會很有助于提高敏感性并評估是否符合出院標準。
參考文獻:
1. Wu F, Zhao S, Yu B, et al. A new coronavirus associated with human respiratory disease in China. Nature 2020; 579:265–9.
2. Phan LT, Nguyen TV, Luong QC, et al. Importation and human-to-human transmission of a novel coronavirus in Vietnam. N Engl J Med 2020; 382:872–4.
3. Holshue ML, DeBolt C, Lindquist S, et al. First case of 2019 novel coronavirus in the United States. N Engl J Med 2020; 382:929–36.
4. Rothe C, Schunk M, Sothmann P, et al. Transmission of 2019-nCoV infection from an asymptomatic contact in Germany. N Engl J Med 2020; 382:970–1.
5. World Health Organization. WHO Director-General’s opening remarks at the media briefing on COVID-19—28 February 2020. Available at:
https://www.who.int/dg/speeches/detail/who-director-general-s-openingremarks-at-the-media-briefing-on-covid-19---28-february-2020. Accessed27 February 2020.
6. Li Q, Guan X, Wu P, et al. Early transmission dynamics in Wuhan, China, of novel coronavirus-infected pneumonia. N Engl J Med 2020; 382:1199–207.
7. World Health Organization. Coronavirus disease 2019 (COVID-19) situation report-39. Available at: https://www.who.int/docs/default-source/coronaviruse/situation-reports/20200228-sitrep-39-covid-19.pdf ?sfvrsn=5bbf3e7d_2. Accessed 28 February 2020.
8. World Health Organization. Laboratory testing for 2019 novel coronavirus (2019-nCoV) in suspected human cases. Available at: https://www.who.int/publications-detail/laboratory-testing-for-2019-novel-coronavirus-in-suspectedhuman-cases-20200117. Accessed 19 March 2020.
9. National Health Commission of the People’s Republic of China website. Diagnosis and treatment of novel coronavirus pneumonia (trial version sixth). Available at: http://www.nhc.gov.cn/yzygj/s7653p/202002/8334a8326dd94d329df351d7da8aefc2.shtml. Accessed 19 February 2020.
10. Winichakoon P, Chaiwarith R, Liwsrisakun C, et al. Negative nasopharyngeal and oropharyngeal swab does not rule out COVID-19. J Clin Microbiol 2020. doi:10.1128/JCM.00297-20
11. Wu J, Liu J, Zhao X, et al. Clinical characteristics of imported cases of COVID-19 in Jiangsu Province: a multicenter descriptive study. Clin Infect Dis 2020. doi:10.1093/cid/ciaa199
12. Huang JT, Liu YJ, Wang J, et al. Next generation digital PCR measurement of hepatitis B virus copy number in formalin-fixed paraffin-embedded hepatocellular carcinoma tissue. Clin Chem 2015; 61:290–6.
13. Gupta RK, Abdul-Jawad S, McCoy LE, et al. HIV-1 remission following CCR5Δ32/Δ32 haematopoietic stem-cell transplantation. Nature 2019; 568:244–8.
14. Ji JS, Wei TM, Yang WB, et al. Early signs and differential diagnosis of CT in novel coronavirus pneumonia. 2020. Available at: http://book.sciencereading.cn/shop/book/Booksimple/show.do?id=B9EEB25369BD13E47E053020B0A0AEEF0000.Accessed February 2020.
15. Dobnik D, Kogov?ek P, Jakomin T, et al. Accurate quantification and characterization of adeno-associated viral vectors. Front Microbiol 2019; 10:1570.
16. Hindson CM, Chevillet JR, Briggs HA, et al. Absolute quantification by droplet digital PCR versus analog real-time PCR. Nat Methods 2013; 10:1003–5.
17. Chan JF, Yuan S, Kok KH, et al. A familial cluster of pneumonia associated with the 2019 novel coronavirus indicating person-to-person transmission: a study of a family cluster. Lancet 2020; 395:514–23.
18. Pan Y, Zhang D, Yang P, Poon LLM, Wang Q. Viral load of SARS-CoV-2 in clinical samples. Lancet Infect Dis 2020; 20:411–2.
19. Zou L, Ruan F, Huang M, et al. SARS-CoV-2 viral load in upper respiratory specimens of infected patients. N Engl J Med 2020; 382:1177–9.
20. Lan L, Xu D, Ye G, et al. Positive RT-PCR test results in patients recovered from COVID-19. JAMA 2020. doi:10.1001/jama.2020.2783
21. Peiris JS, Chu CM, Cheng VC, et al; HKU/UCH SARS Study Group. Clinical progression and viral load in a community outbreak of coronavirus-associated SARS pneumonia: a prospective study. Lancet 2003; 361:1767–72.
上海伯杰醫療科技有限公司是一家致力于感染性病原體分子診斷試劑研發和應用,深耕于多重熒光PCR診斷試劑和痕量病毒二代測序試劑及相關服務的國家高新技術企業。公司圍繞感染性病原體這一主線,從診斷試劑、診斷儀器、測序服務和醫檢所服務等多個面提供全套解決方案。公司秉承“勇于創新,質量為先”的方針,為醫療機構、疾控公衛、高校科研等合作伙伴提供優質產品與服務。

全國客服電話:400-860-3688















.jpg)